이번 강의는 이후 모든 유기 반응을 이해하는 데 기초가 되는 핵심 개념들이 등장한다.
특히 첨가‧제거‧치환‧자리옮김이라는 네 가지 반응 종류는 앞으로 배울 메커니즘의 기본 틀이 되므로 확실히 개념을 잡아두는 것이 중요하다.
유기 반응을 분류하는 네 가지 큰 틀
전 세계 연구자들이 발견한 수많은 유기 반응은 결국 4가지 범주로 정의할 수 있다.
- 첨가 반응(Addition)
- 제거 반응(Elimination)
- 치환 반응(Substitution)
- 자리옮김 반응(Rearrangement)
이 네 가지 분류만 정확히 이해해도 유기화학 책 수백 페이지를 구조적으로 바라볼 수 있게 된다.
첨가 반응(Addition Reaction)
● 핵심 개념
다중 결합(이중·삼중결합)을 가진 분자에 다른 물질이 붙어 하나의 새로운 분자로 합쳐지는 반응이다.
출발물질 + 반응물 → 하나의 생성물
2가지 물질이 반응 후에는 한 가지 물질로 변하면서 모두 단일 결합으로 바뀌는 경우가 많다. (2 가지 물질 → 1 가지 물질로)
첨가반응은 제거반응의 반대 개념이다.

이중결합이나 삼중결합을 가진 알켄·알킨이 일반적인 반응 대상이다.
다중결합은 전자 밀도가 높기 때문에 외부에서 들어오는 분자가 쉽게 첨가된다.
→ 다중 결합을 가진 분자는 “무언가 붙을 준비가 된 상태”라고 이해하면 된다.
제거 반응(Elimination Reaction)
● 핵심 개념
첨가 반응의 역반응
한 분자에서 두 개의 원자나 작용기가 떨어져 나가 두 개의 생성물이 생긴다.(1 가지 물질 → 2 가지 물질로)
제거된 부분에 의해 새로운 이중결합이 만들어지는 경우가 많다. (단일결합 → 제거 → 이중결합 형성)
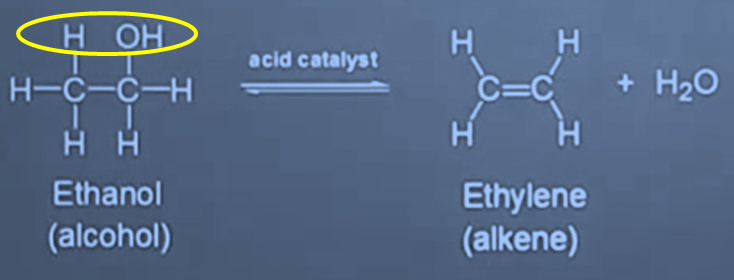
한 분자에서 –H와 –OH가 제거되면 물(H₂O)이 떨어져 나가고, 남은 탄소 사이에 이중결합이 생긴다.
● 특징
출발물질 : 단일결합 위주
생성물 : 이중결합 또는 새로운 다중결합 형성
흔히 E1, E2 반응으로 배우는 과정들이 여기에 포함된다.
치환 반응(Substitution Reaction)
● 핵심 개념
분자 내에 있는 특정 원자나 작용기가 다른 것으로 교체되는 반응이다.
물질의 개수는 반응 전후로 변하지 않는다. (2 가지 물질 → 2 가지 물질로)

메테인(CH₄)의 H 하나가 Cl로 바뀌는 것처럼 결합 하나가 끊어지고 새로운 결합이 생기며 분자 내 구성 원자가 “바뀌는” 반응이다.
● 용어
유기화학에서는 대표적으로
SN1, SN2
SE(전자친화성 치환)
SR(기타 치환)
등으로 치환 반응을 분류해 사용한다.
앞의 ‘S’가 substitution(치환)을 의미한다.
자리옮김 반응(Rearrangement Reaction)
● 핵심 개념
분자 안에 있던 작용기 또는 결합 위치가 이동하는 반응이다.
출발물질과 생성물 모두 1종, 즉 물질의 개수 변화가 없다. (1 가지 물질 → 1 가지 물질로)
단순히 “자리만 바뀐 상태”

탄소 4개짜리 분자에서 말단 탄소에 있던 이중결합이 산 촉매 조건에서 시간이 지나면 옆 탄소로 이동하는 경우가 있다.
이처럼 작용기 혹은 결합 위치가 재배치되는 반응이 자리옮김 반응이다.

● 중요한 특징
독립적으로 일어나기도 하지만, 첨가·제거·치환 반응이 진행될 때 함께 일어나는 경우가 매우 많다.
즉, 유기 메커니즘을 그릴 때 가장 성가시지만 실제 반응에서는 매우 자주 등장하는 동반 반응이다.
'■ 기초화학 > ▷ 유기화학' 카테고리의 다른 글
| 2025년 올해의 분자로 "벤젠(Benzene)"이 선정! 유기화학을 대표하는 벤젠 발견 200주년 (0) | 2025.12.21 |
|---|---|
| 유기화학 제5강 입체화학, 거울상 이성질체란 무엇이고 물리적·화학적 성질의 차이는? (1) | 2025.12.06 |
| 유기화학 제4강 사이클로알케인(Cycloalkane)과 사이클로알케인의 명명법(Nomenclature) 및 입체화학 (0) | 2025.12.02 |
| 유기화학 제3강 알케인과 입체화학, 주요 유기화학 작용기(Functional group) (0) | 2025.11.27 |
| 유기화학 2강 극성 공유 결합(전기음성도, 극성 공유결합, 쌍극자 모멘트) (0) | 2025.11.27 |