거울상 이성질체란?
- 정의 : 분자가 중심 탄소(흔히 키랄 탄소, chirality center)를 가질 때, 그 탄소에 결합한 4개의 치환기(치환기 A, B, C, D)가 모두 서로 다르면 그 탄소는 거울상 이성질체를 만들 수 있다.
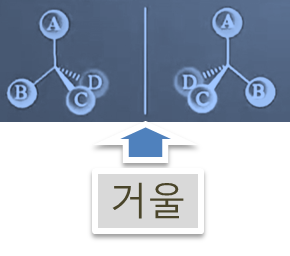
- 특징 : 두 분자는 서로의 거울상처럼 보이지만 겹쳐지지 않음 → 서로 다른 화합물로 취급된다.
사람의 왼손과 오른손처럼 대칭적이지만 중첩 불가한 관계다.
거울상 이성질체가 생기기 위한 조건

중심 탄소는 sp³ 혼성 상태(정사면체)여야 한다.
그 탄소에 결합한 4개의 치환기가 서로 달라야 한다.
위 두 조건이 충족될 때 거울상 이성질체(쌍)가 존재한다.
거울상 이성질체 예시와 판별법
평면 도형을 입체로 그려서, 거울에 비춰본 상과 비교한다.
또는 분자를 180° 회전시켜 같은 배열인지 확인한다.

예 : A·B·C·D라는 치환기가 있을 때, 회전 후 특정 치환기 위치가 서로 반대이면 거울상 관계임을 확인할 수 있다.
A·B·C·D를 각각 할로겐 원소(예: F, Cl, Br)와 수소(H)로 치환하여 입체그림과 이를 180° 회전해 위치 변화 확인해보라.
거울상 이성질체 물리적·화학적 성질의 차이
거울상 이성질체는 대부분의 물리적 성질(녹는점, 끓는점, 밀도 등)은 비슷하다.
그러나 광학적 성질(고유 광회전도, optical rotation)만 부호가 반대다.
예 : 한 쪽이 +1.02°라면 대응하는 엔안티오머는 −1.02°를 갖는다.
화학적 반응성도 비키랄 환경(예: 효소, 편광성 시약)에서는 큰 차이를 보일 수 있다.
거울상 이성질체는 중심 탄소의 네 치환기가 모두 다를 때 나타나는 현상으로, 외형은 서로의 거울상이지만 겹쳐지지 않으며 광회전도에서만 부호가 반대인 특징을 가진다.
'■ 기초화학 > ▷ 유기화학' 카테고리의 다른 글
| 2025년 올해의 분자로 "벤젠(Benzene)"이 선정! 유기화학을 대표하는 벤젠 발견 200주년 (0) | 2025.12.21 |
|---|---|
| 유기화학 제6강 유기 반응의 개요(첨가, 제거, 치환, 자리옮김) (1) | 2025.12.08 |
| 유기화학 제4강 사이클로알케인(Cycloalkane)과 사이클로알케인의 명명법(Nomenclature) 및 입체화학 (0) | 2025.12.02 |
| 유기화학 제3강 알케인과 입체화학, 주요 유기화학 작용기(Functional group) (0) | 2025.11.27 |
| 유기화학 2강 극성 공유 결합(전기음성도, 극성 공유결합, 쌍극자 모멘트) (0) | 2025.11.27 |