바나듐, 사실 고대부터 인간에게 알려져 있었다!
바나듐은 고대부터 알려진 원소였지만 현대 과학자들에 의해 그 유용성이 제대로 발견되었다.
바나듐 자체를 '독립된 원소'로 알고 있었던 건 아니지만, 바나듐이 들어간 광물은 고대부터 다양한 문명에서 사용되고 있었다.
아즈텍 문명 - 바나듐 함유 강철
멕시코 지역에서 번성했던 아즈텍(Aztec) 문명은 "특별히 단단한 강철 무기"를 제작한 것으로 유명하다.
이들 금속에는 자연적으로 바나듐(V)과 티타늄(Ti)이 소량 섞여 있었다.
바나듐은 철과 결합할 때 강도를 크게 높여준다. 즉, 아즈텍인들은 '왜' 그렇게 강한지는 몰랐지만, 바나듐 함유 광석을 가공해서 무기를 만들고 있었던 것이다.
고대 중국 - 바나듐 청동
춘추전국시대(기원전 770~221년) 중국에서는 바나듐이 미량 들어간 청동 합금이 발견된 바 있다. 당시 사람들은 이 성질을 인식하고 귀한 그릇이나 무기 제작에 사용했다.
(물론, 그 안에 바나듐이 있다는 건 몰랐다.)
바나듐은 자연계에서 보통 티타늄광석(Ilmenite, 이르메나이트)이나 자철석(Magnetite) 같은 광물에 소량 섞여 존재한다.
이런 광물을 고대인들이 채굴하고 사용했기 때문에, 바나듐도 자연스럽게 문화 속에 스며들어 있었다.

바나듐은 주로 광물 자원으로부터 채굴된다. 특히 남아프리카, 러시아, 중국 등이 주요 생산지이다.
바나듐(Vanadium), 어떻게 발견됐을까?
1801년, 멕시코에 살던 스페인계 과학자 안드레스 마누엘 델 리오(Andrés Manuel del Río)가 처음 바나듐을 발견했으나 그 당시 유럽에서는 새로운 원소를 인정받으려면 매우 엄격한 검증을 거쳐야 했는데, 델 리오의 발견은 제대로 주목받지 못했다.
30년쯤 뒤인 1830년, 스웨덴의 화학자 닐스 가브리엘 쇠플스트룀(Nils Gabriel Sefström)이 전혀 다른 광석을 분석하다가 '새로운 금속'을 다시 발견했다.
쇠플스트룀은 이 신비로운 원소에 "바나듐(Vanadium)"이라는 이름을 붙였다.
쇠플스트룀은 이 원소의 특이한 색 변화에 주목했다. 그리고 신중하게 실험을 반복한 끝에, 이것이 확실히 기존 원소들과 다르다는 걸 증명했다.
이 이름은 북유럽 신화에 나오는 사랑과 아름다움의 여신 바나디스(Vanadis)에서 따온 것이다. (아마 다양한 색을 띠는 성질 때문에 '아름다운' 여신 이름을 붙인 것으로 보인다.)
바나듐(Vanadium)의 화학적 특성
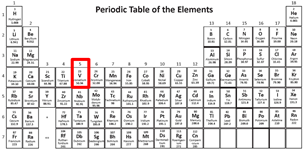
- 원소 기호 V, 원소 번호 23, 원자 질량 약 50.9415 u
- 주기율표 위치는 4주기, 5족 (이전 명칭으로는 5B족)
- 고체 (회색빛 금속)
- 단단하고 연성이 있으며, 다양한 산화수를 가진다

바나듐의 가장 큰 특징 중 하나는 -1부터 +5까지 다양한 산화수(oxidation state)를 자유롭게 오갈 수 있다는 것이다.
23번 원소 바나듐은 철(Fe, 26번)과 매우 가까운 위치에 있어서 금속 결합 특성과 화학적 반응성이 둘 다 뛰어나다. 또, 3d 전자 오비탈에 전자가 세 개 들어가 있어서 산화수 조절이 자유롭다. (이게 배터리나 촉매에서 중요한 이유다.)

→ 이처럼 바나듐은 전자 하나만 왔다 갔다 해도 색깔과 성질이 확 바뀐다.
색상 변화에 따라 다양한 바나듐 화합물이 존재한다. 빨강, 녹색, 파랑, 황색 등 다양한 색조를 띄고 있어 안료로 활용된다.
바나듐은 왜 중요한가?

1. 바나듐은 오늘날 강철 합금에 필수적으로 쓰인다. (강도와 내식성을 높여준다.)
합금에 소량의 바나듐을 첨가하면 그 합금의 강도와 탄성을 획기적으로 높일 수 있다. 이러한 특성으로 자동차 산업 등 다양한 분야에서 중요한 원료로 사용된다. 그리고 고온에서 강도와 내구성을 유지하기 때문에 산업현장에서 매우 유용하다. 또한 독특한 광택을 가지고 있어 금속 재료로 인기 있으며 비행기나 우주선의 초경량 합금으로 많이 사용하고 있다.
2. 리튬이온 배터리 대형화 버전인 바나듐 레독스 플로우 배터리(VRFB) 에도 활용된다.
바나듐 레드옥스 플로우 배터리(VRFB)는 바나듐의 산화수 변화를 이용해서 전기를 저장하고 꺼내 쓸 수 있는 대형 배터리 시스템이다.
이게 바로 VRFB(Vanadium Redox Flow Battery)다.
(특히 재생 에너지 저장 분야에서 주목받고 있다.)
3. 촉매(Catalyst)
바나듐은 화학반응을 빠르게 하거나 효율을 높이는 촉매(catalyst) 역할에서도 엄청난 존재감을 가진다.
가장 대표적인 예는 바로 황산 생산 공정이다.

<접촉법(Contact Process) - 바나듐 오키사이드>
황산(H₂SO₄)은 산업적으로 엄청나게 중요한 화학물질이다.
이 황산을 대량 생산할 때 이산화황(SO₂)을 삼산화황(SO₃)으로 산화시켜야 하는데, 이 과정에서 V2O5(바나듐산화물)가 촉매로 쓰인다.
바나듐이 촉매로 들어가면 반응 속도가 빨라지고 낮은 온도에서도 생산성이 좋아진다.
또 다른 촉매 분야로는 석유 정제(중질유에서 황을 제거하는 반응), 유기 합성 반응(특정 화합물 선택적 산화)에도 바나듐 기반 촉매가 많이 쓰인다.
4. 생화학(생체 화학)에서도 주목
바나듐은 생체 내에서는 일부 조류나 해양 생물에서 '미량 필수 원소' 역할을 한다는 연구도 있다.
바나듐은 사람의 인체에 꼭 필요한 미량 원소 중 하나이다.
뼈 건강과 인슐린 작용에 부분적으로 기여하고 있고 특정 효소의 활성화에도 매우 중요하다. 또한 인슐린 유사 작용(insulin-mimetic effect)이 있다는 연구 결과도 있어서, 당뇨병 치료 연구에도 바나듐 화합물이 관심을 받고 있다.
일부 조개류나 해조류 같은 해양 생물에서 효소의 보조 인자(cofactor) 역할을 한다.
'■ 기초화학 > ▷ 원소 이야기' 카테고리의 다른 글
| 화학이 가장 사랑하지만, 동시에 뼈까지 녹일 정도로 가장 두려워하는 원소 “불소(Fluorine)” (0) | 2025.09.16 |
|---|---|
| 팔라듐(Pd)이란 무엇이며 특별한 능력(수소와 산소를 결합시키는 촉매 역할) 물의 생성 과정 최초 촬영 성공 (0) | 2025.06.30 |
| 붕소(Boron; B)의 재미있는 발견 이야기와 붕소의 과학적 산업적 가치와 쓰임새 (0) | 2025.04.13 |
| 베릴륨(Beryllium; Be)은 어떤 원소일까? 베릴륨 발견, 특징, 독성, 주요 용도, 주의할 점까지 종합 정리 (0) | 2025.04.10 |
| 원소 주기율표의 역사: 과학 혁명의 퍼즐을 맞추다 (0) | 2025.03.24 |